MODELO DE DALTON 1803
– Define por primera vez el átomo como la partícula más pequeña (indivisible) de la materia.
– Los átomos de un mismo elemento son idénticos y tienen las mismas propiedades.
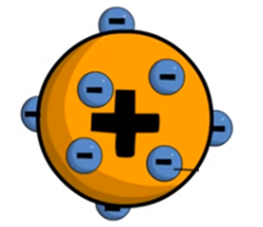
MODELO DE THOMSON 1904
– Descubre los electrones y los define como partículas con carga negativa.
– Propone que el átomo es una esfera uniforme de materia cargada positivamente con electrones incrustados.
– El átomo es neutro ya que la carga positiva se compensa con la carga negativa.
(modelo pastel de pasas)
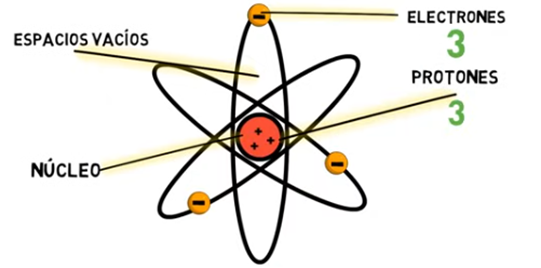
MODELO DE RUTHERFORD 1911
– Descubre que el átomo tiene un núcleo con partículas carga positiva (protones) que contiene la mayoría de la masa del átomo.
– Propone que los electrones se mueven por su alrededor como lo hacen los planetas alrededor del sol.
(modelo planetario)
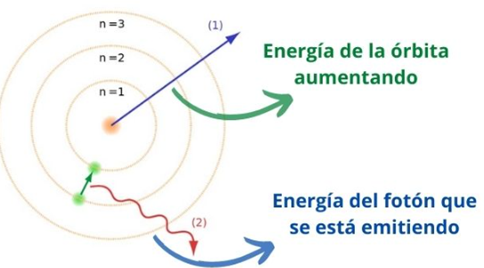
MODELO DE BOHR 1913
– Descubre que el electrón orbita en círculos y que en cada órbita tiene una cantidad de energía.
– El electrón puede cambiar de órbitas y en cada salto emite o absorbe energía.